3'-Amínó-2'-hýdroxý-[1,1'-bífený]-3-karboxýlsýra
3'-Amínó-2'-hýdroxý-[1,1'-bífený]-3-karboxýlsýra
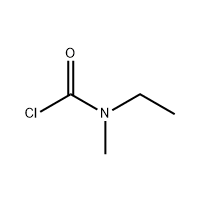
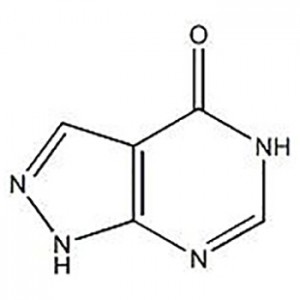
3'-Amínó-2'-hýdroxý-[1,1'-bífený]-3-karboxýlsýra er notuð sem milliefni Eltrombopag.
Eltrombopag, þróað af GlaxoSmithKline (GSK) í Bretlandi og síðar þróað í sameiningu með Novartis í Sviss, er fyrsti og eini viðurkenndur lítill sameinda non-peptíð TPO viðtakaörvi í heiminum.Eltrombopag var samþykkt af bandaríska matvæla- og lyfjaeftirlitinu árið 2008 til að meðhöndla sjálfvakinn blóðflagnafæð purpura (ITP) og árið 2014 til meðferðar á alvarlegu vanmyndunarblóðleysi (AA).Það er einnig fyrsta lyfið sem bandaríska FDA hefur samþykkt til meðferðar á AA undanfarin 30 ár.
Í desember 2012 samþykkti bandaríska matvælastofnunin Eltrombopag til að meðhöndla blóðflagnafæð hjá sjúklingum með langvinna lifrarbólgu C (CHC), þannig að lifrarbólgu C sjúklingar með slæmar horfur vegna lágs blóðflagnafjölda geta hafið og viðhaldið stöðluðu interferónmeðferð við lifrarsjúkdómum.Þann 3. febrúar 2014 tilkynnti GlaxoSmithKline að Matvæla- og lyfjaeftirlitið veitti byltingarkennda lyfjaprófið Eltrombopag til að meðhöndla blóðfæð hjá sjúklingum með alvarlegt efnisblóðleysi (SAA) sem svöruðu ekki ónæmismeðferð að fullu.Þann 24. ágúst 2015 samþykkti bandaríska matvælastofnunin Eltrombopag til meðferðar á blóðflagnafæð hjá fullorðnum og börnum 1 árs og eldri með langvarandi ónæmisblóðflagnafæð (ITP) sem hafa ófullnægjandi svörun við barksterum, immúnóglóbúlínum eða miltistöku.Þann 4. janúar 2018 var Eltrombopag samþykkt til að vera skráð í Kína til að meðhöndla frumónæmisblóðflagnafæð (ITP).


![3'-Amínó-2'-hýdroxý-[1,1'-bífený]-3-karboxýlsýra Valin mynd](http://cdn.globalso.com/jindunchem-med/image351.png)
![3'-Amínó-2'-hýdroxý-[1,1'-bífený]-3-karboxýlsýra](http://cdn.globalso.com/jindunchem-med/image351-300x300.png)
![6-tetra-O-aktýl-1-C-[4-klór-3-[[4-[[(3S)-tetrahýdrófúran-3-ýl]oxý]fenýl]](http://cdn.globalso.com/jindunchem-med/0ecf55f0-300x300.jpg)